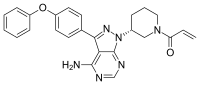
ଇବ୍ରୁଟିନିବ
 | |
| Clinical data | |
|---|---|
| Trade names | Imbruvica, others |
| Synonyms | PCI-32765, CRA-032765 |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a614007 |
| data | |
| Pregnancy category | |
| Routes of administration | By mouth (capsules) |
| Legal status | |
| Legal status | |
| Pharmacokinetic data | |
| Protein binding | 97.3% |
| Metabolism | Liver (CYP3A & CYP2D6) |
| Elimination half-life | 4–6 hours |
| Excretion | Feces (80%), urine (10%) |
| Identifiers | |
| |
| ECHA InfoCard | 100.232.543 |
| Chemical and physical data | |
| Formula | C25H24N6O2 |
| Molar mass | ୪୪୦.୫୧ g·mol−1 |
| 3D model (JSmol) | |
| |
| |
ଇବ୍ରୁଟିନିବ, ଅନ୍ୟମାନଙ୍କ ମଧ୍ୟରେ ଏକ ବେପାର ନାମ ଇମ୍ବ୍ରୁଭିକା, ହେଉଛି ଏକ ଔଷଧ ଯାହା ମାଣ୍ଟଲ ସେଲ ଲିମ୍ଫୋମା (ଏମସିଏଲ/MCL), କ୍ରୋନିକ୍ ଲିମ୍ଫୋସାଇଟିକ ଲ୍ୟୁକେମିଆ (ସିଏଲଏଲ/CLL) ଏବଂ ୱାଲଡେନଷ୍ଟ୍ରୋମର ମାକ୍ରୋଗ୍ଲୋବୁଲିନେମିଆ ରୋଗମାନଙ୍କର ଚିକିତ୍ସା ପାଇଁ ବ୍ୟବହୃତ ହୁଏ ।[୫] [୨] ଏମସିଏଲ ଓ ସିଏଲଏଲ ରୋଗରେ ଅନ୍ୟ ସମସ୍ତ ଚିକିତ୍ସା ବିଫଳ ହେଲେ ଏହି ଔଷଧ ବ୍ୟବହୃତ ହୁଏ ।[୨] ଗ୍ରାଫ୍ଟ ବନାମ ହୋଷ୍ଟ ରୋଗରେ ମଧ୍ୟ ଏହି ଔଷଧ ଦିଆଯାଏ ।[୫] ଏହା ପାଟିରେ ଦିଆଯାଏ ।[୫]
ସାଧାରଣ ପାର୍ଶ୍ୱ ପ୍ରତିକ୍ରିୟାରେ ଥ୍ରୋମ୍ବୋସାଇଟୋପେନିଆ, ନିମ୍ନ ଲୋହିତ ରକ୍ତ କଣିକା ସ୍ତର, କମ୍ ଶ୍ୱେତ ରକ୍ତ କଣିକା ସ୍ତର, ତରଳ ଝାଡ଼ା, ରାସ, ରକ୍ତସ୍ରାବ ଏବଂ ପାଟି ପ୍ରଦାହ ହୋଇପାରେ ।[୫] ଅନ୍ୟ ପାର୍ଶ୍ୱ ପ୍ରତିକ୍ରିୟାରେ ସଂକ୍ରମଣ, ହୃଦ୍ପାତ, ଉଚ୍ଚ ରକ୍ତଚାପ, ଅନ୍ୟାନ୍ୟ କର୍କଟ ଏବଂ ଟ୍ୟୁମର ଲାଇସିସ୍ ସିଣ୍ଡ୍ରୋମ ହୋଇପାରେ ।[୫] ଗର୍ଭାବସ୍ଥାରେ ବ୍ୟବହାର କଲେ ଶିଶୁର କ୍ଷତି ହୋଇପାରେ ।[୫] ଏହା ବ୍ରୁଟନର ଟାଇରୋସିନ୍ କାଇନେଜକୁ (BTK) ଅବରୋଧ କରି କାମ କରେ ଯାହାଦ୍ୱାରା ବି ସେଲ୍ ବିଭାଜନ ମନ୍ଥର ହୋଇଯାଏ ।[୨]
ବା୨୦୧୩ ମସିହାରେ ଯୁକ୍ତରାଷ୍ଟ୍ରରେ ଏବଂ ୨୦୧୪ରେ ୟୁରୋପରେ ଡାକ୍ତରୀ ବ୍ୟବହାର ପାଇଁ ଇବ୍ରୁଟିନିବ ଅନୁମୋଦିତ ହୋଇଥିଲା ।[୬] [୨] ବିଶ୍ୱ ସ୍ୱାସ୍ଥ୍ୟ ସଂଗଠନର ଅତ୍ୟାବଶ୍ୟକୀୟ ଔଷଧ ତାଲିକାରେ ଏହାର ନାମ ଉଲ୍ଲେଖ ଅଛି । [୭] ଜେନେରିକ୍ ସଂସ୍କରଣଗୁଡିକ ଅନୁମୋଦିତ ହୋଇଛି ।[୮] ଯୁକ୍ତରାଜ୍ୟରେ 4 ସପ୍ତାହ ଚିକିତ୍ସା ବାବଦ ଖର୍ଚ୍ଚ ୨୦୨୧ ସୁଦ୍ଧା ୫,୦୦୦ ପାଉଣ୍ଡ ଖର୍ଚ୍ଚ ହୋଇଥାଏ ।[୯] ଯୁକ୍ତରାଷ୍ଟ୍ରରେ ଏହି ରାଶିର ମୂଲ୍ୟ ପ୍ରାୟ ୧୪,୫୦୦ ଡଲାର ଅଟେ ।[୧୦]
ଆଧାର
[ସମ୍ପାଦନା]- ↑ "Ibrutinib (Imbruvica) Use During Pregnancy". Drugs.com. 3 December 2019. Archived from the original on 28 March 2020. Retrieved 28 March 2020.
- ↑ ୨.୦ ୨.୧ ୨.୨ ୨.୩ ୨.୪ "Imbruvica EPAR". European Medicines Agency (EMA). 8 July 2021. Archived from the original on 10 April 2021. Retrieved 14 July 2021.
- ↑ "Imbruvica 140 mg Film-Coated Tablets - Summary of Product Characteristics (SmPC)". (emc). 16 January 2020. Archived from the original on 28 March 2020. Retrieved 28 March 2020.
- ↑ "UK Ibrutinib label". UK Electronic Medicines Compendium. 25 August 2016. Archived from the original on 30 July 2019. Retrieved 3 October 2021.
- ↑ ୫.୦ ୫.୧ ୫.୨ ୫.୩ ୫.୪ ୫.୫ ୫.୬ "Imbruvica- ibrutinib capsule Imbruvica- ibrutinib tablet, film coated". DailyMed. 8 April 2020. Archived from the original on 12 August 2020. Retrieved 21 April 2020.
- ↑ "Ibrutinib Monograph for Professionals". Drugs.com (in ଇଂରାଜୀ). Archived from the original on 10 July 2020. Retrieved 24 November 2021.
- ↑ World Health Organization (2021). World Health Organization model list of essential medicines: 22nd list (2021). Geneva: World Health Organization. hdl:10665/345533. WHO/MHP/HPS/EML/2021.02.
- ↑ "Ibrutinib: FDA-Approved Drugs". U.S. Food and Drug Administration (FDA). Archived from the original on 24 June 2021. Retrieved 19 June 2021.
- ↑ BNF 81: March-September 2021. BMJ Group and the Pharmaceutical Press. 2021. p. 1028. ISBN 978-0857114105.
- ↑ "Imbruvica Prices, Coupons & Patient Assistance Programs". Drugs.com (in ଇଂରାଜୀ). Archived from the original on 13 September 2021. Retrieved 24 November 2021.
