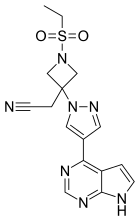
ବାରିସିଟିନିବ
| |||
| Clinical data | |||
|---|---|---|---|
| Trade names | Olumiant, others | ||
| Synonyms | INCB28050, LY3009104 | ||
| AHFS/Drugs.com | monograph | ||
| MedlinePlus | a618033 | ||
| data |
| ||
| Pregnancy category | |||
| Routes of administration | By mouth (tablets) | ||
| Legal status | |||
| Legal status | |||
| Pharmacokinetic data | |||
| Bioavailability | 79% | ||
| Protein binding | 50% | ||
| Metabolism | CYP3A4 (<10%) | ||
| Elimination half-life | 12.5 hours | ||
| Excretion | 75% urine, 20% faeces | ||
| Identifiers | |||
| |||
| ECHA InfoCard | 100.219.080 | ||
| Chemical and physical data | |||
| Formula | C16H17N7O2S | ||
| Molar mass | ୩୭୧.୪୨ g·mol−1 | ||
| 3D model (JSmol) | |||
| |||
| |||
ବାରିସିଟିନିବ, ଅନ୍ୟମାନଙ୍କ ମଧ୍ୟରେ ଏକ ବେପାର ନାମ ଓଲୁମିଆଣ୍ଟ, ଏକ ଔଷଧ ଯାହା ରିମାଟଏଡ୍ ଆର୍ଥ୍ରାଇଟିସ୍ (RA) ଏବଂ କୋଭିଡ-୧୯ (COVID-19)ର ଚିକିତ୍ସା ପାଇଁ ବ୍ୟବହୃତ ହୁଏ । [୫] [୬] ରିମାଟଏଡ୍ ଆର୍ଥ୍ରାଇଟିସରେ ଏହା ବ୍ୟବହୃତ ହୁଏ ଯେତେବେଳେ ଏହା ନେକ୍ରୋସିସ୍ ଫ୍ୟାକ୍ଟର୍ (TNF) ଇନହିବିଟରଦ୍ୱାରା ନିୟନ୍ତ୍ରିତ ହୁଏନି । [୫] କୋଭିଡ-୧୯ର ଗୁରୁତର ରୋଗରେ ବ୍ୟବହୃତ ହୁଏ । [୬] ଏହା ପାଟିରେ ଦିଆଯାଏ । [୪]
ସାଧାରଣ ପାର୍ଶ୍ୱ ପ୍ରତିକ୍ରିୟାରେ ବାନ୍ତି, ଉପର ଶ୍ୱାସନଳୀ ସଂକ୍ରମଣ, ହର୍ପିସ ଜୋସ୍ଟର, ଏବଂ ହର୍ପିସ୍ ସିମ୍ପଲେକ୍ସ ହୋଇପାରେ । [୭] ଅନ୍ୟାନ୍ୟ ପାର୍ଶ୍ୱ ପ୍ରତିକ୍ରିୟାରେ ଭୟଙ୍କର ସଂକ୍ରମଣ, ଲିମ୍ଫୋମା, ରକ୍ତ ଜମାଟ ବାନ୍ଧିବା, ଜଠରାନ୍ତ୍ର ଛିଦ୍ର, ଏବଂ ଯକୃତ ସମସ୍ୟା ଅନ୍ତର୍ଭୁକ୍ତ ହୋଇପାରେ । [୭] ଗର୍ଭାବସ୍ଥାରେ ବ୍ୟବହାର କରୁଥିବା କୌଣସି ତଥ୍ୟ ନାହିଁ, ଯଦିଓ ଅନ୍ୟ ପ୍ରାଣୀମାନଙ୍କରେ ବ୍ୟବହାର ଶିଶୁର କ୍ଷତି କରିପାରେ । [୭] ଏହା ଜାନୁସ୍ କିନାସେ (JAK)ର ଏକ ପ୍ରତିରୋଧକ, ଜେଏକେ୧ ଏବଂ ଜେଏକେ୨ ଉପ ପ୍ରକାରକୁ ଅବରୋଧ କରିଥାଏ । [୮]
୨୦୧୭ ମସିହାରେ ୟୁରୋପରେ ଏବଂ ୨୦୧୮ରେ ଆମେରିକାରେ ଡାକ୍ତରୀ ବ୍ୟବହାର ପାଇଁ ଅନୁମୋଦିତ ହୋଇଥିଲା । [୪] [୫] ଯୁକ୍ତରାଜ୍ୟରେ ୨ ମିଗ୍ରାର ୨୮ ବଟିକାର ମୂଲ୍ୟ ୨୦୨୧ରେ ୮୦୦ ପାଉଣ୍ଡ ଥିଲା । [୯] ଯୁକ୍ତରାଷ୍ଟ୍ରରେ ଏହି ରାଶିର ମୂଲ୍ୟ ପ୍ରାୟ ୨,୩୦୦ ଡଲାର ଥିଲା । [୧୦]
ଆଧାର
[ସମ୍ପାଦନା]- ↑ ୧.୦ ୧.୧ "Olumiant Product Information" (PDF). Therapeutic Goods Administration (TGA). Archived from the original on 20 September 2021. Retrieved 12 June 2021.
- ↑ "Baricitinib (Olumiant) Use During Pregnancy". Drugs.com. 8 November 2019. Archived from the original on 26 June 2020. Retrieved 16 March 2020.
- ↑ "AusPAR: Baricitinib". Therapeutic Goods Administration (TGA). 20 May 2021. Archived from the original on 20 May 2021. Retrieved 11 June 2021.
- ↑ ୪.୦ ୪.୧ ୪.୨ "Olumiant EPAR". European Medicines Agency (EMA). 3 December 2019. Archived from the original on 25 August 2021. Retrieved 1 September 2021. Text was copied from this source which is © European Medicines Agency. Reproduction is authorized provided the source is acknowledged.
- ↑ ୫.୦ ୫.୧ ୫.୨ ୫.୩ "Olumiant- baricitinib tablet, film coated". DailyMed. 13 November 2019. Archived from the original on 27 September 2020. Retrieved 16 March 2020.
- ↑ ୬.୦ ୬.୧ "Hospitalized Adults: Therapeutic Management". COVID-19 Treatment Guidelines (in ଇଂରାଜୀ). Archived from the original on 9 January 2022. Retrieved 8 January 2022.
- ↑ ୭.୦ ୭.୧ ୭.୨ "Baricitinib Monograph for Professionals". Drugs.com (in ଇଂରାଜୀ). Archived from the original on 21 September 2021. Retrieved 8 January 2022.
- ↑ "Summary of opinion for Olumiant" (PDF). European Medicines Agency (EMA). 15 December 2016. Archived from the original (PDF) on 15 March 2018. Retrieved 1 September 2021.
- ↑ BNF 81: March-September 2021. BMJ Group and the Pharmaceutical Press. 2021. p. 1153. ISBN 978-0857114105.
- ↑ "Olumiant Prices, Coupons & Patient Assistance Programs". Drugs.com (in ଇଂରାଜୀ). Archived from the original on 22 January 2021. Retrieved 8 January 2022.